Энзим
Энзим (Фермент) бол эсийн дотор химийн урвалыг хурдасгах үйл ажиллагааг явуулдаг уургийн молекул юм[1]. Ферментүүд нь биед явагдах химийн урвалыг хурдасгадаг боловч тухайн үйл явцыг бүрэн дүүрэн хянадаггүй.
Амьд биед явагдах ихэнх биохимийн урвалд ферментүүд шаардлагатай байдаг. Ферментийн оролцоотой урвалууд бусад урвалаас хурдан явагддаг.
Урвалын эхэнд оролцож байгаа химийн бодисыг субстрат гэж нэрлэдэг. Энэ субстратууд нь химийн урвалын эцэст урвалын бүтээгдэхүүн болж хувирдаг. Өөрөөр хэлбэл фермент субстратуудтай ажиллаж тэдгээрийг бүтээгдэхүүнд хувиргадаг.
Ферментийн бүтэц
засварлахХимийн бүтцийн хувьд ферментүүд уураг учир олон амин хүчлээс тогтсон өндөр молекулт нэгдэл юм. Эдгээр амин хүчлүүд нь пептидийн холбоогоор хоорондоо урт гинжилсэн байдалтай холбогдож, улмаар энэ гинж нугарч мушгирч, нарийн нийлмэл бүтцийг үүсгэдэг.
Ферментүүдэд субстраттай холбогдох хэсэг байдаг. "сарвуу, ан, хонхорхой, гүдгэр зэргээр тухайн молекулд атгах, барих, тэлэх, нугалах зэргээр үйлчлэл үзүүлдэг".[2]p37
Мянга мянган өөр ферментүүд байдаг. Ферментүүдийн нэр нь тэдгээрийг ямар фермент болохыг нь илтгэдэг. Ферментийн нэрс гол төлөв –ase төгсгөлтэй байх ба энэ тухайн нэрийн цаана фермент байгааг илэрхийлдэг. Жишээ нь, ATP synthase гэж нэртэй фермент байхад уг фермент ATP(гурван фосфорт аденазин)-ийг нийлэгжүүлдэг фермент гэж ойлгогдоно. Өөр нэг жишээ татахад ДНХ полимераза (DNA polymerase) гэдэг фермент нь ДНХ-ийн хуучин хэлхээг ашиглан шинэ хэлхээг нийлэгжүүлдэг.
Шүлсний амилаза фермент нь цардуулын том молекулыг задалж глюкоз ба мальтозын жижиг молекул болгодог байхад өөр нэг төрлийн Лифаза ферментүүд өөх тосны молекулыг жижиг молекулд хувиргадаг гэх мэт олон жишээ татаж болно. Протеазууд бол ферментийн нэгэн анги бөгөөд тэдгээр нь бусад фермент ба уургийг задалж амин хүчилд хувиргадаг.[3]
Ферментүүд нь том химийн бодисыг жижиг химийн бодист хувиргаад зогсохгүй эсрэгээр жижиг химийн бодисоос том нийлмэл химийн бодис үүсгэх болон бусад химийн хувирлуудыг мөн гүйцэтгэдэг. Ферментүүдийн ангилал нь доор бичигдсэн үндсэн хэлбэрүүдэд хуваагддаг.
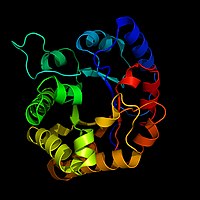
Биохимичид ферментийг зургийг загвар үзүүлэн хэрэглэн зурдаг. Ферментийн дотор олон мянган атом байх учир бүрэн дүрслэхэд хүндрэлтэй байдаг. Биохимичид ферментийг бүрэн нарийвчлан дүрслэхийн оронд туузан загварыг ашигладаг. Туузан загвар нь ферментэд байх атом бүрийг үзүүлэхгүйгээр ферментийн ерөнхий хэлбэрийг төлөөлөн харуулдаг.
Ихэнх ферментүүд тохирсон температур ба рН орчингүйгээр ажиллахгүй. Сүүгээр бойжигч амьтдын биеийн дулаан 37oC хэм байдаг тул ихэнх ферментийн ажиллах хэм болдог. Харин pH-ийн хувьд нилээд өргөн хүрээтэй. Жишээ нь, Пепсин нь pH 1.5 орчим байхад ажилладаг.[4]
Тухайн нэг температурын босгоос хэтрүүлэн халаахад ферментийг дахиж сэргэхгүйгээр эвддэг. Хэрэв фермент протеазын нөлөөгөөр задарсан бол түүний бүрэлдэхүүн химийн бодисыг дахин хэрэглэж болдог.
Зарим химийн бодис ферментийн үйл ажиллагааг дэмжиж болдог. Эдгээрийг идэвхжүүлэгч (активатор) гэж нэрлэдэг. Ферментийн үйлчлэлийг удаашруулах болон зогсох үйлчилгээтэй бодисууд байдгийг саатуулагч (ингибитор) гэж нэрлэдэг. Ихэнх эм нь хүний биед байгаа ферментүүдийг хурдасгах болон удаашруулах үйлчилгээтэй химийн бодисууд байдаг.
Үйл ажиллагаа
засварлахАливаа ферментэт урвалын ерөнхий тэгшитгэл нь:
- Субстрат + Фермент –> Субстрат:Фермент –> Бүтээгдэхүүн:Фермент –> Бүтээгдэхүүн + Фермент
Жишээ нь, Сахараза нь түүний субстрат болох сахарозоос 400 дахин том бөгөөд сахарозыг түүнийг бүрдүүлэгч моносахарууд болох глюкоз ба фруктоз болгон задалдаг. Сахараза сахарозыг нугалан глюкоз, фруктозын хоорондох химийн холбоог хүчлэн салгадаг. Үүн дээр усны молекул холбогдож хоёр хэсгийг бүрэн салгадаг. ферментүүд нь дараах үндсэн шинж чанаруудтай байдаг:
- Тэдгээр нь урвалыг хурдасгах чанартай. ферментүүд урвалын эрчмийг 10 сая дахин нэмэгдүүлдэг.[2]p39 Урвалын явцад фермент өөрөө өөрчлөгддөггүй.
- Ферментүүд жижиг хэмжээтэй байсан ч үйлчлэлтэй. Нэг ферментийн молекул 1000 субстратын молекулыг нэг минутад хувиргаж болох ба зарим фермент нэг минутад 3 сая субстратыг хувиргадаг.[2]p39
- Тэдгээр нь ихээхэн өвөрмөц. Нэг фермент тухайн субстратаас явагдаж болох олон урвалаас зөвхөн нэгийг явуулдаг.
Ферментийн идэвхийг хянах
засварлахФерментийн идэвхийг эсийн түвшинд хянадаг таван үндсэн арга зам байдаг.
- Эсийн орчин өөрчлөгдөхөд ферментийн нийлэгжлийг (тухайн ферментийн генийн транскрипц ба трансляци) ихэсгэж багасгаж болдог. Генийн зохицуулгын энэ хэлбэрийг ферментийн индукц ба ингибиц гэж нэрлэдэг. Жишээ нь, пенициллин зэрэг антибиотикт тэсвэртэй бактер пенициллиний молекулыг задралд оруулдаг ферментийг нийлэгжүүлдэг.
- Ферментүүд эсийн өөр өөр хэсгүүдэд тохиолдож болно. Жишээ нь, өөхний хүчил эсийн цитозол, эндоплазмын тор, гольджийн аппаратад байх нэг хэсэг ферментүүдийн үйл ажиллагааны үр дүнд нийлэгжээд митохондрид байх арай өөр хэсэг бүлэг ферментийн үйлчлэлээр энергийн эх үүсвэр бий болдог.[5]
- Ферментүүд өөрсдийн бүтээгдэхүүнээрээ зохицуулагдаж болдог. Жишээ нь эсийн бүтээгдэхүүн тухайн бодисын нийлэгжих замын эхний ферментүүдийн нэгийг дарангуйлдаг. Бүтээсэн эцсийн бүтээгдэхүүний хэмжээгээр түүний өөрийн концентраци зохицуулагддаг учир ийм зохицуулгын зарчмыг сөрөг буцалттай гэж нэрлэдэг. Энэ нь эцсийн бүтээгдэхүүнийг хэтэрхий их хэмжээгээр үйлдвэрлэхээс хамгаалдаг. Ферментийн үйл ажиллагааны энэ хяналт нь амьд биеийн тогтвортой дотоод орчин буюу гоместазыг хэрэгжүүлэхэд тусалдаг.
- ферментүүд урвалыг явуулсныхаа дараа өөрчлөгдөх байдлаар зохицуулагдаж болно. Жишээ нь полипептидийн гинж тасрах. Хоол боловсруулахад оролцодог протеазе болох химотрипсин нойр булчирхайд байхдаа идвэхигүй хэлбэрт байж байгаад ходоодонд орохдоо идэвхждэг. Энэ нь тэр ферментийг нойр булчирхай ба нарийн гэдсэнд орохын өмнө бусад эдийг гэмтээхээс хамгаалдаг. Ферментийн анхны идэвхгүй хэлбэрийг зимоген гэдэг.
- Зарим фермент өөр орчинд (Өндөр pH тайгаас бага pH тай орчинд) шилжихдээ идэвхжиж болдог. Жишээ нь, томуугийн вируcын хемагглютинин хэлбэр өөрчлөгдөхөд идэвхиждэг. Энэ хэлбэрийн өөрчлөлт нь эзэн эсийн лизосомын дотор ороход орчны хүчиллэг өөрчлөгдөхөөс хамаардаг.[6]
Кофакторууд
засварлахКофакторууд буюу коэзимүүд нь урвалыг явуулахад шаардлагатай туслагч молекулууд юм. тэдгээр нь уургийн бус органик ба органик бус молекулууд байдаг. Энэ төрлийн молекулууд нь заримдаа Mg2+, Cu2+, Mn2+, төмөр-хүхэр багцаар гэх мэт металлын ионыг төвдөө агуулдаг. Эдгээр металл электрон донорын үүрэгтэй учир олон урвалын хувьд маш чухал байдаг. Витамин гэх мэт олон төрлийн ферментийн жижиг туслагчууд ийм л үндсэн шалтгааны улмаас амьтдад хэрэгцээтэй байдаг.[7][8]
Ангилал зүй
засварлахБиохимийн олон улсын холбоо (International Union of Biochemistry)-ны ферментийн комисс нээгдээд байгаа бүх ферментүүдийг зургаан бүлэгт хуваасан. Үүнд:
- ОксидоРедуктаза: электрон зөөвөрлөхийг хурдасгадаг
- Трансферазууд: нэг молекулаас нөгөөд функционал бүлгийг зөөдөг
- Гидролазууд: –OH (гидроксил)-ийн бүлгийг нэмдэг
- Лиазууд: химийн холбоонуудыг салгаж шинэ давхар холбоо эсвэл цагираг бүтцийг үүсгэдэг
- Изомеразууд: A –> B Эндээс B нь A гийн изомер болдог.
- Лигазууд: Хоёр том молекулыг нэгтгэдэг: Ab + C –> A–C + b
Тухайн нэг фермент тэдгээрийн ангилал зүйгээс хамаарсан дөрвөн тоогоор нэрлэгддэг.[9]p145[10]
Эшлэл
засварлах- ↑ Concise Oxford Dictionary.
- ↑ 2.0 2.1 2.2 Kornberg, Arthur 1989. For the love of enzymes: the odyssey of a biochemist. Harvard. ISBN 0-674-30775-5
- ↑ Pugh, Maureen Barlow (ed) 2000. Stedman's medical dictionary, 27th ed. Baltimore, Maryland, USA: Lippincott, Williams & Wilkins. p65
- ↑ "Effects of pH". Татаж авсан: 2010-04-29.
- ↑ Faergeman NJ, Knudsen J (1997). "Role of long-chain fatty acyl-CoA esters in the regulation of metabolism and in cell signalling". Biochem. J. 323 (Pt 1): 1–12. PMC 1218279. PMID 9173866.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Carr C.M. & Kim P.S. (2003). "A spring-loaded mechanism for the conformational change of influenza hemagglutinin". Cell. 73: 823–32. doi:10.1016/0092-8674(93)90260-W. PMID 8500173.
{{cite journal}}: Unknown parameter|month=ignored (help) - ↑ Sauke, David J.; Metzler, David E. and Carol M. 2001. Biochemistry: the chemical reactions of living cells. 2nd ed, Harcourt/Academic Press, San Diego. ISBN 0-12-492540-5
- ↑ Bugg, Tim 1997. An introduction to enzyme and coenzyme chemistry. Blackwell, Oxford. ISBN 0-86542-793-3
- ↑ King R.C. Stansfield W.D. & Mulligan P.K. 2006. A dictionary of genetics, 7th ed. Oxford.
- ↑ Enzyme database [1]